Einfluss von Palmitoylethanolamid auf chronische Schmerzen
Diese systematische Übersichtsarbeit mit Metaanalyse untersucht die Wirksamkeit und Verträglichkeit von Palmitoylethanolamid (PEA) bei chronischen Schmerzen. Basierend auf 11 doppelblinden, randomisierten, kontrollierten Studien mit insgesamt 774 Patient: innen zeigt sich, dass PEA im Vergleich zu Placebo oder aktiven Kontrollen eine signifikante Reduktion der Schmerzintensität bewirken kann. Der durchschnittliche Unterschied betrug −1,68 Punkte auf einer standardisierten 11-Punkte-Skala. Zusätzlich berichten einige Studien über positive Effekte auf Lebensqualität, Schlaf und Funktionalität. Unerwünschte Wirkungen waren kaum vorhanden.
Studiendaten
Studienart | Meta-Analyse |
Evidenzgrad | hoch |
Grundlage der Studie | doppelblinde randomisierte kontrollierte Studien (11) mit insgesamt 774 Personen |
Erscheinungsjahr | 2023 |
Journal | Nutrients |
Erstautorin | Lang-Illievich K. |
PMID | 36986081 |
Einleitung
Chronische Schmerzen betreffen weltweit hunderte Millionen Menschen und stellen eine enorme Belastung für die Lebensqualität sowie das Gesundheitssystem dar. Zu den häufigsten Formen zählen muskuloskelettale Schmerzen (z. B. Arthrose, Rückenschmerzen), neuropathische Schmerzen (z. B. diabetische Polyneuropathie) und funktionelle Schmerzsyndrome (z. B. Reizdarmsyndrom, Fibromyalgie). Diese Zustände gehen oft mit psychischen Belastungen wie Depression, Angst oder Schlafstörungen einher und erfordern multimodale Therapieansätze.
Die verfügbaren medikamentösen Optionen – wie NSAR, Opioide oder Antikonvulsiva – sind in ihrer Wirksamkeit limitiert und mit relevanten Nebenwirkungen verbunden. Gerade bei langandauernder Einnahme kann es zu Problemen wie gastrointestinalen Beschwerden, kardiovaskulären Risiken oder Abhängigkeitsentwicklung kommen.
Vor diesem Hintergrund wächst das Interesse an sogenannten „neuroprotektiven“ oder endogen wirksamen Substanzen wie Palmitoylethanolamid (PEA). PEA ist ein körpereigenes Fettsäureamid, das zur Gruppe der Endocannabinoid verwandten Lipide gehört. Es wirkt nicht direkt an den klassischen Cannabinoid-Rezeptoren CB1 und CB2, entfaltet aber über PPAR-α, TRPV1 und andere Signalwege entzündungshemmende, neuroprotektive und analgetische Effekte.
Ursprünglich wurde PEA bereits in den 1950er-Jahren als Bestandteil von Eigelb und Sojalecithin identifiziert und in der ehemaligen Tschechoslowakei unter dem Handelsnamen Impulsin zur Infekt-Prophylaxe eingesetzt. Erst in den letzten zwei Jahrzehnten erlebte PEA ein wissenschaftliches Comeback im Bereich der Schmerzmedizin. Zahlreiche präklinische Studien und kleinere klinische Arbeiten deuten auf eine Wirksamkeit bei chronischen Schmerzsyndromen hin. Bisher fehlte jedoch eine methodisch fundierte, aktuelle Synthese der vorhandenen klinischen Evidenz.
Ziel der vorliegenden Arbeit war es daher, die Effektivität und Sicherheit von PEA anhand doppelblinder, randomisierter, kontrollierter Studien systematisch zu bewerten und durch eine Metaanalyse zu quantifizieren.
Materialien und Methoden
Die Literaturrecherche erfolgte systematisch in den Datenbanken MEDLINE und Web of Science. Zusätzlich wurde Google Scholar als ergänzende Quelle genutzt und Referenzlisten relevanter Übersichtsarbeiten wurden manuell durchsucht. Studienregistrierungen wurden ebenfalls geprüft (clinicaltrials.gov). Die finale Suche wurde am 1. Januar 2023 abgeschlossen.
Eingeschlossen wurden nur doppelblinde, randomisierte, kontrollierte Studien (RCTs), die PEA in jeglicher Formulierung, Dosierung und Dauer untersuchten – allein oder in Kombination mit anderen Substanzen. Vergleichsarme waren entweder Placebo oder aktive Kontrolltherapien. Die Zielpopulation waren erwachsene Patient: innen mit chronischen Schmerzen, definiert als Schmerzen über mehr als drei Monate. Als primärer Endpunkt diente die Schmerzintensität – unabhängig von der verwendeten Skala (z. B. VAS, NRS, Likert).
Sekundäre Endpunkte waren Lebensqualität, funktioneller Status sowie Nebenwirkungen. Es wurde ein Random-Effects-Modell für die Metaanalyse verwendet, um der zu erwartenden Heterogenität zwischen den Studien Rechnung zu tragen. Die Datenextraktion und Bewertung erfolgten durch zwei unabhängige Gutachter, mit einem dritten Prüfer zur Konfliktlösung.
Die methodische Qualität der Studien wurde anhand des klassischen und modifizierten Jadad-Scores bewertet. Nur Studien mit Jadad ≥3 und modifiziertem Jadad ≥5 wurden in die Metaanalyse eingeschlossen. Zusätzlich wurde das Risiko für Bias nach dem RoB-2-Tool der Cochrane Collaboration eingeschätzt. Ein Sensitivitätsanalyse wurde durchgeführt, um den Einfluss potenziell verzerrter Studien auf das Gesamtergebnis zu prüfen.
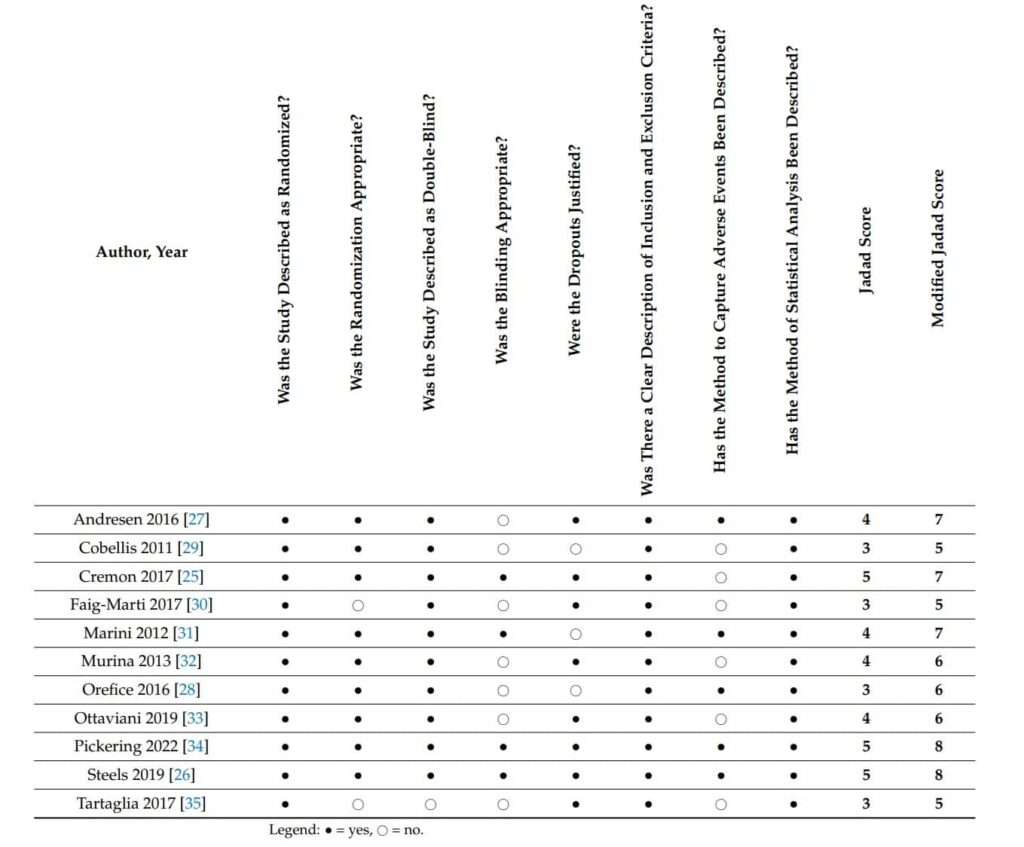
Abbildung 1 Auflistung der JADAD Sub Scores der analysierten Studien. Die Studien, die in die Meta-Analyse miteinbezogen wurden, haben alle einen ausreichend hohen Jadad Score und sind daher aufgrund ihrer hohen methodischen Qualität gut geeignet.
Resultate
Aus 253 identifizierten Publikationen erfüllten 11 Studien (n = 774) die Einschlusskriterien. Die meisten Studien stammten aus Italien, Australien und anderen europäischen Ländern. Die behandelten Indikationen reichten von neuropathischen Schmerzen über muskuloskelettale Beschwerden bis hin zu gynäkologischen Schmerzsyndromen.
Abbildung 2 Zentrale Ergebnisse der inkludierten Studien. In der Abbildung sind die Tagesdosierungen von PEA sowie die die Ergebnisse der Studien angeführt, die in die Meta-Analyse integriert wurden. Es ist vor allem angeführt, dass es nur bei einer Studie zu Nebenwirkungen gekommen ist, die anderen Studien haben keine unerwünschte Arzneimittelwirkungen mit der Behandlung von PEA in Verbindung gebracht.
PEA zeigte in der gepoolten Analyse eine signifikante Reduktion der Schmerzintensität im Vergleich zu Placebo oder aktiver Kontrolle (mittlere Differenz: −1,68; 95 % CI: −2,31 bis −1,05; p = 0,00001). Diese Wirkung war konsistent über verschiedene Indikationen und Populationen hinweg, wenngleich die Heterogenität hoch war (I² = 93 %).
Abbildung 3 Einfluss von PEA auf die Schmerzintensität. Durch die Anwendung von PEA kann gezeigt werden, dass es bei einem Großteil der Patienten zu einer Reduktion der Schmerzintensität kommt. Die Heterogenität der analysierten Daten war allerdings hoch.
In mehreren Studien wurde zudem eine Verbesserung der Lebensqualität, Funktionalität (z. B. Bewegungseinschränkung) und psychischen Begleitfaktoren wie Schlaf und Stimmung festgestellt. Die Verträglichkeit war durchweg gut. Es wurden keine schwerwiegenden Nebenwirkungen berichtet; lediglich eine Studie erwähnte milde gastrointestinale Beschwerden.
Die Behandlungsdauer variierte stark zwischen den Studien: Einige führten die Therapie über nur 10–14 Tage durch, andere über mehrere Wochen bis hin zu einem Jahr. Besonders die längeren Beobachtungszeiträume zeigten eine nachhaltige Schmerzreduktion. Dies spricht dafür, dass PEA in einer Langzeitanwendung möglicherweise eine stärkere Wirkung entfaltet als bei kurzfristiger Gabe.
Was die Dosierung betrifft, schwankten die eingesetzten Mengen zwischen 300 mg und 1200 mg pro Tag. Es wurde sowohl einmal täglich als auch zweimal täglich dosiert. Eine klare Dosis-Wirkungs-Beziehung konnte nicht nachgewiesen werden, was möglicherweise an der unterschiedlichen Bioverfügbarkeit oder Galenik (z. B. Mikronisierung) liegt. Auch hier besteht Bedarf für standardisierte Vergleichsstudien.
Interessant ist außerdem, dass die Form der PEA-Präparate (mikronisiert, ultra-mikronisiert oder nicht modifiziert) keinen klaren Vorteil in Bezug auf die Wirksamkeit zeigte. Zwei gut konzipierte Studien mit nicht mikronisiertem PEA konnten vergleichbare Effekte nachweisen, was die Notwendigkeit teurer Spezialformulierungen infrage stellt.
Einige methodische Unterschiede (z. B. Mikronisierung des Wirkstoffs, Dosierung und Behandlungsdauer) erschweren direkte Vergleiche. In zwei Studien war PEA nicht wirksam, was möglicherweise mit zu niedriger Dosierung oder methodischen Schwächen zusammenhängt. Dennoch blieb in der Gesamtschau der Nutzen von PEA klar erkennbar.
Bewertung der Datenqualität (Reliabilität)
Die eingeschlossenen Studien wiesen insgesamt eine gute methodische Qualität auf (durchschnittlicher modifizierter Jadad-Score 6,4/8). Die meisten Studien waren korrekt verblindet und randomisiert, die Endpunkte klar definiert. Allerdings wurden einige Studien von Herstellern finanziert oder erhielten das Prüfpräparat gestellt – was potenzielle Interessenskonflikte darstellen kann, auch wenn diese inhaltlich nicht zu verzerrten Ergebnissen führten. Die hohe Heterogenität spricht für unterschiedliche Studiensettings, mindert aber nicht grundsätzlich die Aussagekraft. Insgesamt ist die Evidenz als solide, aber nicht abschließend zu bewerten.
Zusammenfassung
Die vorliegende Metaanalyse bietet fundierte Hinweise auf die Wirksamkeit von PEA zur Behandlung chronischer Schmerzen. Die Substanz zeigte in den meisten Studien eine klinisch relevante Schmerzreduktion und wurde gut vertragen. Auch sekundäre Aspekte wie Lebensqualität und körperliche Funktion profitierten teilweise von der Behandlung.
Trotz der ermutigenden Ergebnisse bleibt der genaue Stellenwert von PEA im therapeutischen Spektrum chronischer Schmerzen noch zu klären. Insbesondere fehlen große, unabhängige Studien mit standardisierter Dosierung, definierter Anwendungsdauer und direktem Vergleich verschiedener galenischer Formen (z. B. mikronisiert vs. nicht-mikronisiert). Für die klinische Praxis scheint PEA aktuell vor allem als additive Therapieoption für Patient: innen mit unzureichender Schmerzlinderung und guter Verträglichkeit relevant.
Ihre Fragen, unsere Antworten
Palmitoylethanolamid (PEA) ist ein körpereigener Stoff mit schmerzstillender Wirkung.
In dieser Meta-Analysen wurden die Ergebnisse von 11 klinischen Studien zusammengetragen und es wurde untersucht, ob PEA einen schmerzstillenden Effekt bei chronischen Schmerzen aufweist. Die Studienautoren sind zu der Erkenntnis gekommen, dass PEA im Vergleich zu Placebo oder aktiven Kontrollen eine signifikante Reduktion der Schmerzintensität bewirken kann.
Die Studienautoren haben angeführt, dass es nur bei einer Studie zu milden Nebenwirkungen, vor allem im Magen-Darm-Trakt gekommen ist. Es kann daher als gut verträglich eingestuft werden.
Die analysierten Studien haben unterschiedliche Dosierungen von PEA verwendet. Die Dosierungen waren in einem Bereich zwischen 150 und 600 mg 2xtgl.
Die Studienautoren führen an, dass die Metaanalyse fundierte Hinweise auf die Wirksamkeit von PEA zur Behandlung chronischer Schmerzen bietet. Allerdings müssen weitere Studien klären, die das Thema der Dosierung und die galenische Form (mironisiert oder nicht-mikronisiert) aufgreifen.



