Chronische Schmerzen verstehen
Moderne Ansätze in der Therapieunterstützung
Chronische Schmerzen beeinträchtigen das Leben vieler Menschen nachhaltig auf körperlicher, sowie geistiger Ebene. Trotz verschiedener medikamentöser Optionen ist die therapeutische Zufriedenheit oft gering, insbesondere bei neuropathischen Schmerzen. Palmitoylethanolamid (PEA), ein körpereigenes, fettlösliches Molekül, zeigt in Studien vielversprechende schmerzmodulierende und entzündungshemmende Eigenschaften und ist gleichzeitig sehr gut Verträglich. PEA wirkt über spezifische Rezeptoren und verstärkt körpereigene Schutzmechanismen. Meta-Analysen belegen eine spürbare Schmerzreduktion bei chronischem und akutem Schmerz. Es gibt auch Daten, dass es bei Migräne eingesetzt werden kann. Zudem kann PEA helfen, die Einnahme klassischer Schmerzmittel zu reduzieren. Als sichere, langfristige Option bietet Palmitoylethanolamid eine wertvolle Ergänzung im Schmerzmanagement – besonders für Patienten, die Nebenwirkungen von Medikamenten oder hohen Leidensdruck erfahren.
Einleitung
Die hohe Prävalenz von chronischen neuropathischen Schmerzen wie z.B. Rückenschmerzen hat einen großen Einfluss auf die Lebensqualität von Patientinnen. Schmerz muss möglichst bald therapiert werden, damit er nicht chronifiziert.
Akute Schmerzen sind kurzzeitige, plötzlichen Schmerzen, die z.B. bei Krankheiten, Verletzungen, nach einer Operation oder Geburt empfunden werden.
Chronische Schmerzen sind länger als drei bis sechs Monate anhaltend, führen zu körperlichen Einschränkungen und beeinträchtigen das Befinden, die Stimmung und das Denken.
Durch die Aufnahme von Schmerz in die ICD-11 Klassifikation konnte chronischer Schmerz als eigene Entität erfasst werden. Dadurch wird die Ursache von Schmerz mit unbekannter Herkunft nicht mehr als rein somatisch/psychisch bedingt klassifiziert (1–6).
Quantifizierung von Schmerz
Zur Quantifikation von Schmerz können Skalen verwendet werden, anhand derer das individuelle Schmerzempfinden aufgezeigt werden kann. Eine Reduktion des Schmerzes auf der Skala zeigt die Wirksamkeit einer Therapie an (6).
Pathologie des neuropathischen Schmerzes
Neuropathische Schmerzen entstehen aufgrund einer Nervenschädigung und einer dadurch verringerten Signalübertragung zum Rückenmark. Das führt zu einem veränderten Genexpressionsmuster und einem veränderten Verhalten von Ionenkanälen in der Peripherie. Dadurch entsteht eine ektopischen Aktivität der Nerven, die in weiterer Folge zu Schmerzen führt. Aufgrund der erhöhten neuronalen Aktivität kommt es zu einer erhöhten synaptischen Übertragung, sowie einer verringerten Hemmung auf spinaler und kortikaler Ebene, sowie im Thalamus. Neben den genannten Faktoren kommt es auf allen Ebenen i.e. Peripherie, Rückenmark und Gehirn zu einer Neuro-Inflammation mit Beteiligung von Immunfaktoren wie IL-6, TNF-a, IL-1b sowie zur Erhöhung der Makrophagen-Aktivität (2).
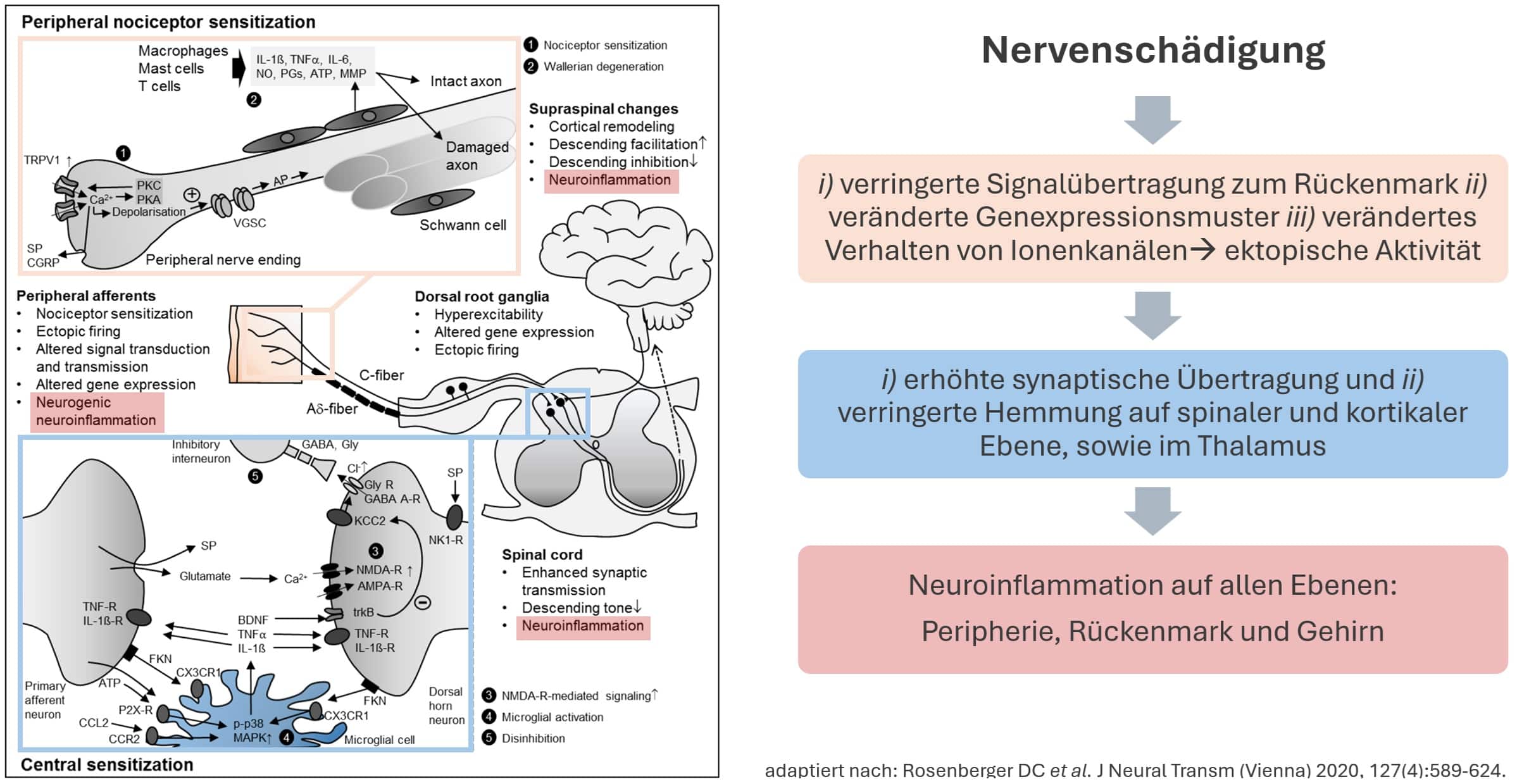
Abbildung 1 Die Pathologie des neuropathischen Schmerzes. Werden Nervenendigungen geschädigt, führt dies zu einer veränderten Signalübertragung zum Rückenmark, was wiederum zu einer Aktivität der Nerven führt, die so an dieser Stelle nicht vorgesehen ist (ektopische Aktivität). Aufgrund der erhöhten Übertragungsrate und verringerten Hemmung von den Nervensignalen kommt es zu einer Entzündungsreaktion auf allen neuronalen Ebenen.
Medikamentöse Behandlung des neuropathischen Schmerzes
Die medikamentöse Behandlung des neuropathischen Schmerzes wird in erster Linie mit trizyklischen Antidepressiva (Amitriptylin), selektiven Serotonin-Noradrenalin-Wieder-aufnahmehemmer (Duloxetin) und den Calciumkanal-alpha-2-delta-Liganden Gabapentin und Pregabalin durchgeführt.
In zweiter Linie wird das schwache Opioid Tramadol in Kombination mit einem nicht-steroidalem-Antirheumatikum angewendet. Nachteile dieser Kombination sind die schwache Studienlage und das hohe Nebenwirkungspotential.
Als dritte Option stehen starke Opioide, weitere Antikonvulsiva, sowie Cannabinoide oder topische Anwendungen wie Lidocain und Capsaicin Pflaster oder Botulinum Toxin Injektionen zur Verfügung.
Die Gruppe der starken Opioide wie Fentanyl oder Buprenorphin sind aufgrund der Nebenwirkungen und geringem Ansprechen nur für Non-Responder reserviert (2).
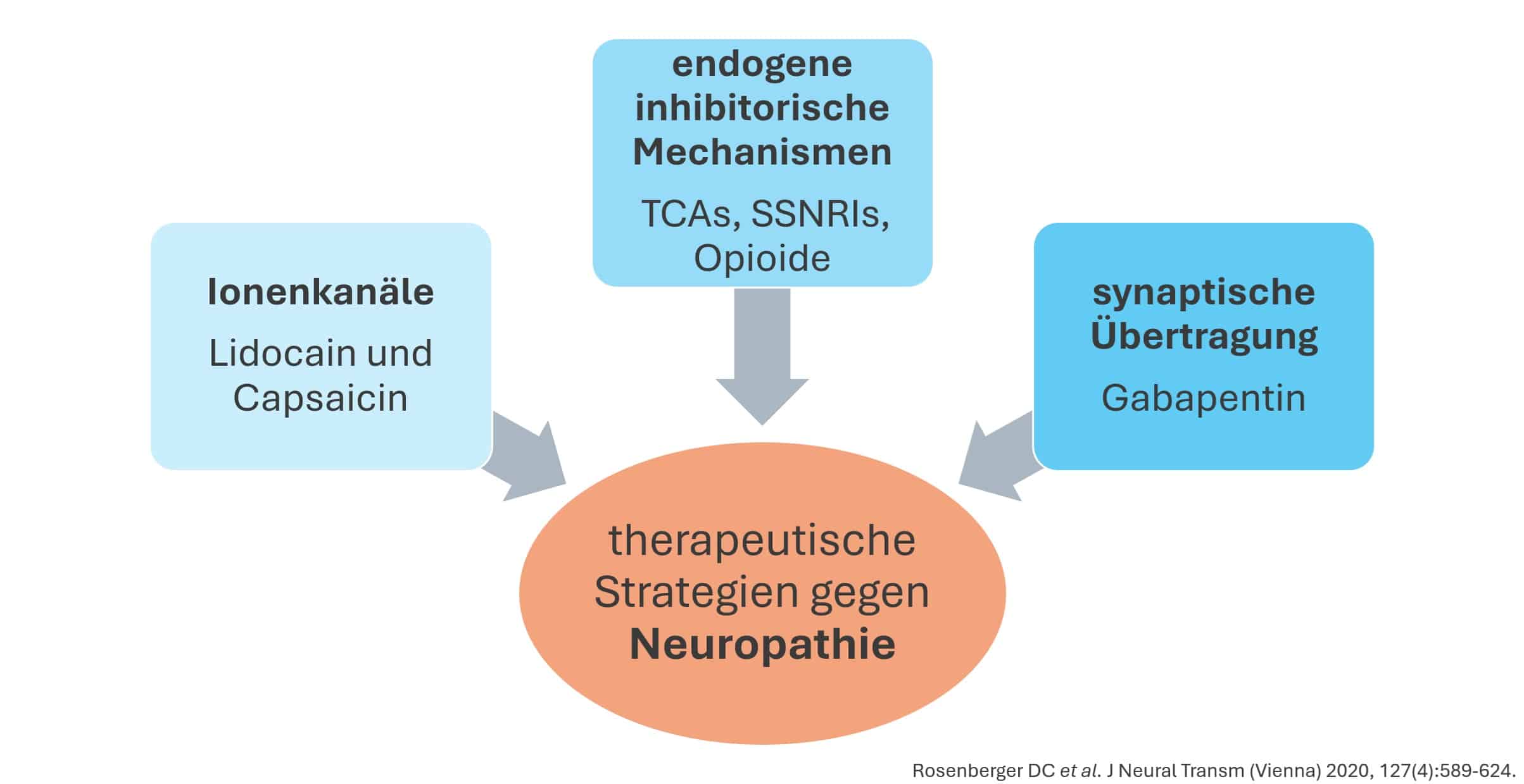
Abbildung 2 Therapeutische Strategien zur Behandlung von neuropathischem Schmerz. Zur Behandlung des neuropathischen Schmerzes werden Substanzen verwendet, die einen Einfluss auf körpereigene hemmende Mechanismen haben oder die Übertragung von Neurotransmittern beeinflussen können. Zur lokalen Therapie werden auch Substanzen verwendet, die einen Einfluss auf Ionenkanäle zeigen.
Therapeutische Lücke
Zu der hohen Anzahl an Patienten kommt hinzu, dass ein Großteil der behandelten Patienten unzufrieden mit ihrer Therapie ist und ein individuelles Ansprechen auf alternative Therapieoptionen und Substanzen durchaus möglich ist. Daher sind personalisierte Therapieansätze für Patienten zur Behandlung von chronischen Schmerzen durchaus gerechtfertigt (2,7).
Vorstellung von Palmitoylethanolamid
Der Wirkstoff Palmitoylethanolamid – auch Palmidrol oder PEA genannt – ist ein lipophiles Fettsäureamid, welches aus Palmitinsäure und Ethanolamin unter Amidbildung das schlecht wasserlösliche Fettsäureamid ergibt. PEA gehört zur Familie der ALIAamide, einer Stoffgruppe, die natürlich vorkommt und als bioaktive Lipide im Körper fungiert. Sie spielen eine Schlüsselrolle in der Regulation von Entzündung, Schmerz und Immunantwort, hauptsächlich über ein Herunterregeln der Aktivität von Mast- und anderen Immunzellen. PEA ist das Bekannteste unter den ALIAmiden (8).
Entdeckung und Vorkommen von PEA
PEA wurde das erste Mal in den 1950er Jahren entdeckt, als erkannt wurde, dass bestimmte Lebensmittel einen entzündungshemmenden Effekt aufzeigen können. Es folgten Untersuchungen am Tiermodell, die den immunmodulatorischen und protektiven Effekt auf unterschiedlichen Gewebearten nachgewiesen haben. In den 1990er Jahren forschte die Nobelpreisträgerin Rita Levi-Montalcini am entzündungshemmenden Mechanismus der ALIAmide. In den 2000er Jahren konnte der analgetische Effekt von PEA erstmals in-vivo gezeigt werden.
PEA kommt ubiquitär in Menschen, Tieren, Pflanzen und Nahrungsmittel vor, wirkt analgetisch, schmerzmodulierend, antiphlogistisch, neuroprotektiv und immunmodulatorisch. Die pharmakologischen Ansatzpunkte von PEA sind die Interaktion mit dem GPR55 und dem TRPV1 Rezeptor, sowie dem nukleären Rezeptor PPARα (8).
Pharmakokinetik von PEA
Die Route und Formulierung von PEA hat einen großen Einfluss auf die Absorption über die Nahrung. Das Distributionsvolumen sowie der präsystemische Katabolismus zeigen noch Fragezeichen in der Pharmakokinetik von PEA auf. PEA wird in die Zellen aufgenommen und kann dort mit seinen Zielstrukturen interagieren und die pharmakologischen Effekte auslösen. Intrazelluläres PEA wird dann in weiterer Folge auch von der fatty-acid-amide-hydrolase (FAAH) oder der N-acylethanolamine-acid-amidase (NAAA) zu Palmitinsäure und Ethanolamin abgebaut.
Die Palmitinsäure wird entweder über den Stuhl ausgeschieden, in Phospholipide eingebaut oder zur ß-Oxidation freigegeben. Inwieweit PEA auch im Urin aufscheint, ist noch nicht vollständig geklärt, aber aufgrund der schlechten Wasserlöslichkeit, ist der Exkretionsmechanismus über den Stuhl eher wahrscheinlich (9).
Pharmakodynamik von PEA
Aus jüngsten Untersuchungen kann sich folgendes Wirkungsspektrum von PEA ableiten lassen:
- Direkte molekulare Targets (agonistische Tätigkeit auf PPAR-α, GPR55 sowie Bindung an den GPR119 Rezeptor).
- Indirekte Effekte (Entourage Effekt auf CB1 oder CB2 Rezeptoren durch erhöhte Bildung von CB2 mRNA und einer erhöhten Anandamid-Konzentration).
- Durch PEA wird die Bildung von GPR55/CB1 und GPR/CB2 Heterodimeren erhöht, wodurch der Entourage Effekt verstärkt wird.
Durch die vermehrte Präsenz von Anandamid kommt es auch zu einem Calcium-Einstrom über TRPV1 Rezeptoren.
Diese direkten und indirekten Effekte führen dazu, dass chronische Schmerzzustände verbessert werden, (10).
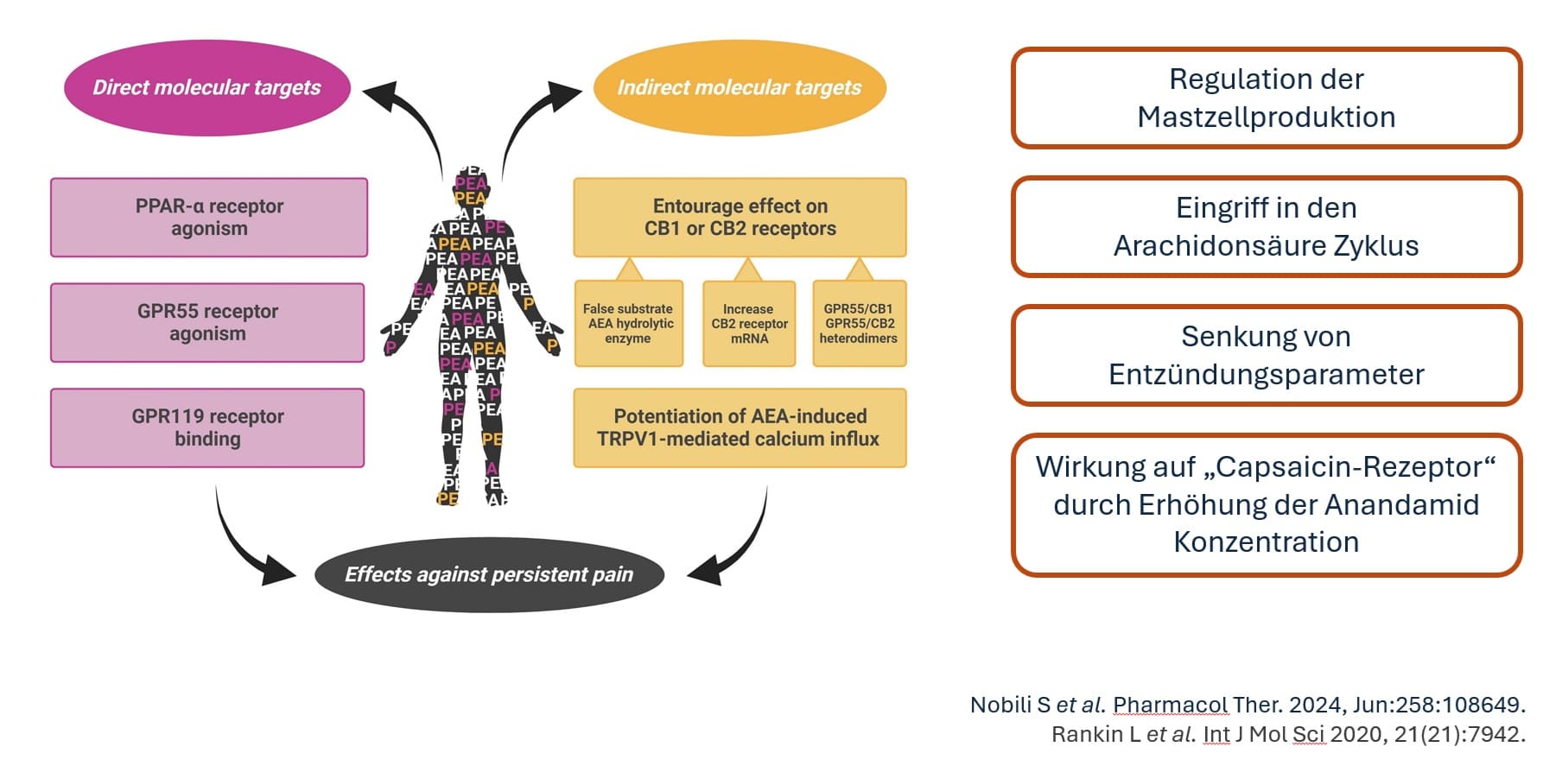
Abbildung 3 Wirkung von Palmitoylethanolamid (PEA) im menschlichen Körper. Die Wirkung von PEA im menschlichen Körper wird nach aktuellem Wissenstand so beschrieben, dass es direkte und indirekte Zielstrukturen gibt, die durch PEA angesteuert werden. Es kommt auf jeden Fall zu einer Regulation der Mastzellproduktion, sowie einem Eingriff in den Arachidonsäure Zyklus, wodurch Entzündungsreaktionen reguliert werden. Aufgrund des indirekten Einflusses auf den „Capsaicin-Rezeptor“ TRPV1 durch Anandamid (AEA) kann der schmerzstillende Effekt von PEA erklärt werden.
Klinische Wirkung von PEA auf Schmerz
Übersichtsarbeit von PEA auf nozizeptiven, muskuloskelettalen und neuropathischen Schmerz
Um die klinischen Effekte von PEA auf nozizeptivem, muskuloskelettalem und neuropathischem Schmerz beurteilen zu können, wurde im Zuge eines systematischen Reviews eine Meta-Analyse durchgeführt (11).
Für die Analyse des schmerzstillenden Effektes wurden 8 Studien herangezogen und die Verringerung der Schmerzintensität mittels nominaler rating scale (NRS) oder visueller Analogskala (VAS) quantifiziert. Bei 6 der 8 Studien konnte ein schmerzstillender Effekt von PEA nachgewiesen werden, bei 2 Studien konnte der schmerzstillende Effekt von PEA in den Daten nicht wiedergefunden werden (positive mittlere Differenz). Bei der Auflistung der einzelnen Studien ist die mittlere Differenz des schmerzstillenden Effektes in den Werten angegeben, in denen die Studie durchgeführt worden ist. Zur Berechnung der totalen mittleren Differenz, wurden die Werte der Studien einander angeglichen, um untereinander vergleichbar sein zu können.
Neben den zwei Studien, die keinen positiven Einfluss von PEA zur Schmerzstillung feststellen konnten, ist die Studienlage mit einem I2 Wert von 99% auch sehr heterogen. Das heißt, dass die analysierten Studien eine hohe methodische Vielfalt aufweisen und die Vergleichbarkeit dadurch erschwert wird.
Mithilfe eines Funnel-Plots kann der Publikations-Bias der untersuchten Studien analysiert werden. Bei einem geringen Publikations-Bias sind die Studien in einem verkehrten Trichter symmetrisch angeordnet. Bei dieser Meta-Analyse sind die Studien eher in dem oberen Bereich lokalisiert, wodurch ein Publikations-Bias vermutet wird.
Allerdings ist bei einer geringen Anzahl an Studien die Aussage des Funnel-Plots nicht sehr hoch, wodurch das Modell selbst nicht genügend Aussagekraft über den Publikations-Bias geben kann. Für die korrekte Analyse werden mindestens 10 Studien benötigt, besser noch sind 20 Studien.
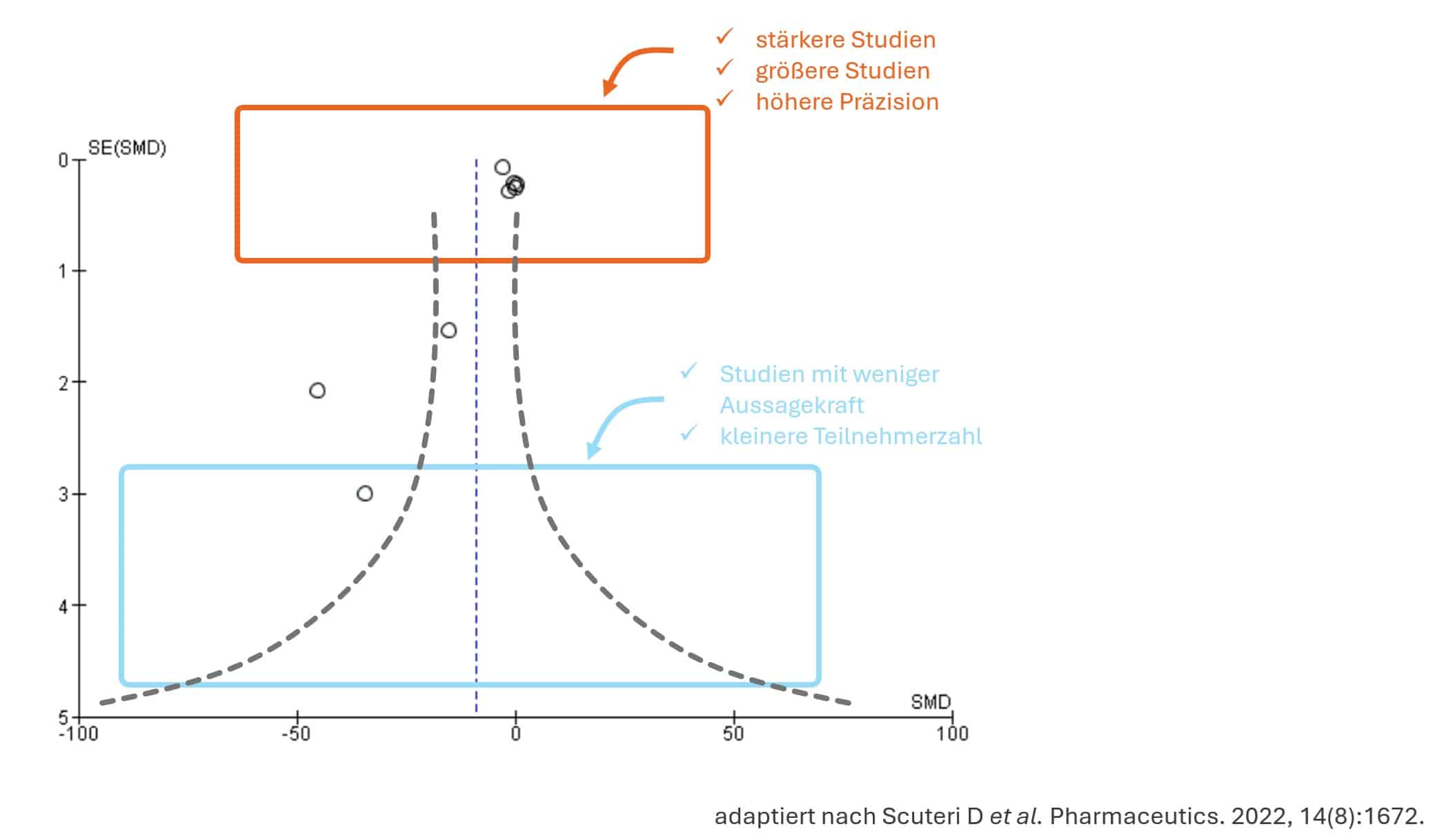
Abbildung 4 Analyse der untersuchten Studien auf Objektivität. Mithilfe eines Funnel-Plots kann analysiert werden, ob die untersuchten Studien objektiv waren, oder ob es zu einer Verzerrung im Zuge der Veröffentlichung (Publikations-Bias) gekommen ist. Damit die Funnel-Plot Analyse auch gelingt, müssen ausreichend Studien zu dem Thema verfügbar sein. In dem konkreten Fall ist eine Tendenz zu Publikations-Bias ersichtlich, allerdings ist die Anzahl an verfügbaren Studien sehr gering und dadurch diese Methode nur bedingt anwendbar.
Obwohl nur eine geringe Anzahl der gefundenen Studien den Kriterien entsprochen hat und nur zwei der Studien RCTs waren, die Heterogenität hoch war und der Funnel-Plot Publikations-Bias nahelegt, konnten doch zwei positive Effekte aus der Studie ausgearbeitet werden.
- Es konnte gezeigt werden, dass es keine PEA assoziierten Drop-outs gegeben hat. Dies zeigt, dass PEA im Allgemeinen gut verträglich ist.
- Außerdem wurde festgestellt, dass die Medikation für Schmerzspitzen verringert werden konnte. Das hat folgende Vorteile für Patienten: i) wird das Risiko für unerwünschte Arzneimittelwirkungen reduziert ii) mit einem geringeren Risiko für unerwünschte Arzneimittelwirkungen geht für ältere Patienten auch ein geringeres Sturzrisiko einher und iii) wird durch die geringere Dosierung das Risiko für Arzneimittelinteraktionen reduziert. Dies ist vor allem für wechselwirkungs-freudige Arzneimittel wie Tramadol, selektive Serotonin Wiederaunahmehemmer (SSNRIs) oder trizyklische Antidepressiva (TCAs) von Wichtigkeit.
Übersichtsarbeit zur Anwendung von PEA bei chronischen Schmerzen
Bei der ersten Meta-Analyse, die wir betrachtet haben, ist der Kritikpunkt angebracht gewesen, dass nur 2 randomisierte kontrollierte Studien (RCTs) in die Analyse zu dem Thema aufgenommen wurden/verfügbar waren. Folgende Meta-Analyse hat den methodischen Vorteil, dass für die Analyse nur RCTs herangezogen wurden und so die Qualität der Studien noch höher ist (12).
Wir haben die Studie aufgrund ihrer Ausführlichkeit in einem separaten Blog Artikel im Zuge eines Journal Clubs hier diskutiert.
Zusammenfassend lässt sich sagen, dass es durch die Anwendung von PEA in einem Dosisbereich von 300-600 mg zu einer Reduktion des Gesamt Schmerz Scores von 1,68 auf einer 11-stelligen Skala gekommen ist.
Die Teilnehmenden Personen haben die Studienmedikation sehr gut vertragen, Nebenwirkungen wurden nur selten und wenn als mild empfunden.
Ein schmerzstillender Effekt ist auch anhand dieser Daten zu erkennen und lässt die Aussage zu, dass PEA zur Verringerung von chronischen Schmerzen herangezogen werden kann.
Wirksamkeit von PEA über einen verlängerten Zeitraum
Für die konkrete Fragestellung, ob PEA zu einem zusätzlichen schmerzstillenden Effekt beiträgt, wenn es über einen Zeitraum von 60 anstelle von 30 Tagen genommen wird, wurden aus insgesamt 116 duplikationsbereinigten Studien 9 Studien identifiziert, die den Suchkriterien der Autoren für folgende Metaanalyse entsprochen haben (13).
Anhand des primären Endpunktes der Studie kann die Frage für die Praxis abgeleitet werden, ob denn nun die Kunden in der Apotheke einen Vorteil aus der verlängerten Einnahme von PEA ziehen können oder nicht. Da PEA als Grundstoff teuer ist und die Adhärenz zu einer Dauertherapie immer wieder Schwierigkeiten für den Endanwender darstellt, ist diese Frage berechtigt.
Die Auswertung lässt den Schluss nahe, dass die Anwendung von PEA über einen längeren Zeitraum auch zu einer größeren Schmerzstillung beitragen kann.
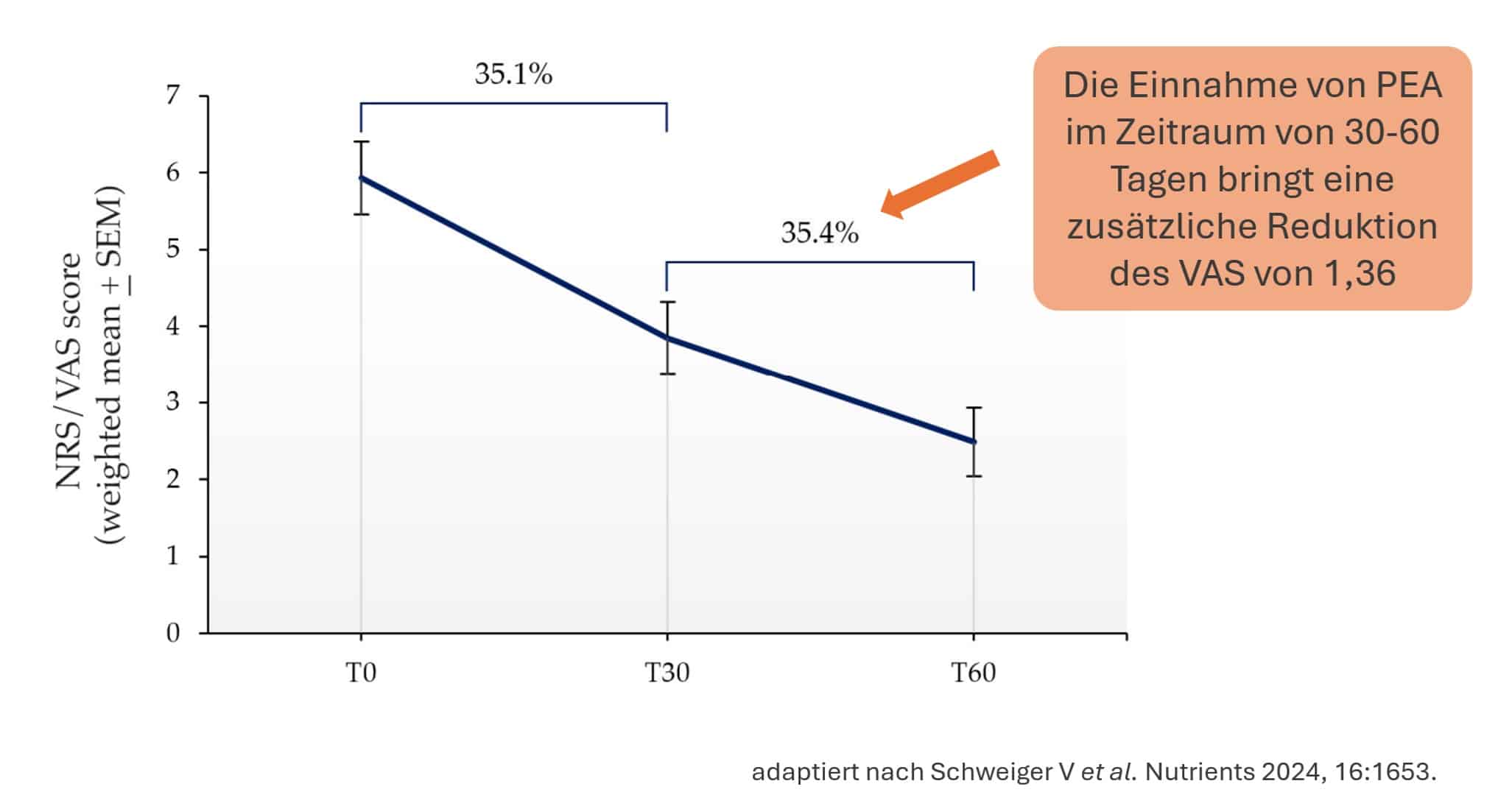
Abbildung 5 Die Einnahme von Palmitoylethanolamid (PEA) über einen verlängerten Zeitraum bringt eine zusätzliche Schmerzreduktion. Die Analyse der betrachteten Studien ergibt, dass Patienten davon profitieren, wenn sie mit PEA behandelt werden. Es konnte auch gezeigt werden, dass eine zusätzliche schmerzstillende Wirkung zustande kommt, wenn PEA über einen längeren Zeitraum (60 Tage) eingenommen wird.
PEA zur Behandlung von Migräne?
In der vorliegenden Studie (14) wurde der Fragestellung nachgegangen, ob es durch die Anwendung von PEA zu einem positiven schmerzstillenden Effekt bei Migräne kommen kann. Es konnte gezeigt werden, dass durch die kurzfristige Einnahme von PEA Migräneattacken schneller aufgelöst werden konnten, im Vergleich zu einem Placebo. Die Forschenden weißen aber auch darauf hin, dass noch größere Studien benötigt werden um die offenen Fragen, vor allem im Hinblick auf Dosierung, Anwendungsdauer und -art beantworten zu können.
Fazit
Palmitoylethanolamid (PEA) zeigt in verschiedenen Studien eine vielversprechende Wirkung zur Linderung chronischer Schmerzen, insbesondere neuropathischer Beschwerden. Es wirkt schmerzstillend, indem es sowohl direkt als auch indirekt in entzündliche und neuronale Prozesse eingreift – unter anderem über Rezeptoren wie PPAR-α, GPR55 und TRPV1. Dabei zeichnet sich PEA durch eine gute Verträglichkeit aus: In den analysierten Studien kam es zu keinen therapiebedingten Abbrüchen, und auch die Rate unerwünschter Nebenwirkungen war niedrig. Besonders vorteilhaft ist, dass PEA über einen längeren Zeitraum sicher angewendet werden kann – Studien zeigen sogar einen zusätzlichen schmerzstillenden Effekt bei einer Einnahme über 60 Tage im Vergleich zu 30 Tagen. Damit stellt PEA eine sinnvolle Ergänzung im therapeutischen Spektrum bei chronischen Schmerzen dar – gerade für Patient:innen, die eine Standardtherapie nicht vertragen oder unzureichend darauf ansprechen.
Ihre Fragen, unsere Antworten
Ja. Chronischer Schmerz wurde in die ICD-11 Klassifikation als eigenständige Erkrankung aufgenommen und wird nicht mehr als rein somatisch/psychisch klassifiziert.
Schmerzen können anhand der visuellen Analogskala (VAS) quantifiziert werden. Eine Reduktion des Schmerzes zeigt den Behandlungserfolg oder Wirksamkeit einer Therapie an.
Neuropathische Schmerzen entstehen aufgrund einer Nervenschädigung und einer dadurch verringerten Signalübertragung zum Rückenmark. Dadurch wird die Aktivität von Genen verändert und es kommt zu einer Entzündung des Nervengewebes mit Beteiligung von Immunfaktoren.
Die medikamentöse Behandlung von neuropathischen Schmerzen erfolgt in erster Linie mit Psychopharmaka und Arzneimittel, die unter anderem auch zur Behandlung von epileptischen Anfällen verwendet werden.
Manche Personen sprechen nicht gut auf die Erstlinientherapie zur Schmerzstillung an oder vertragen die empfohlene/wirksame Dosis der verordneten Arzneimittel nicht. Für solche Patienten kann eine individuelle Therapieempfehlung von Vorteil sein.
Eine systematische Auswertung von mehreren klinischen Studien (Meta-Analyse) konnte zeigen, dass es durch die Anwendung von Palmitoylethanolamid zu einer Reduktion des Schmerzscores (gemessen an der visuellen Analogskala) gekommen ist.
Quellenverzeichnis
- Palomares A, Ryan D, Kelly JO, Bhatt KJ, Garcia-Larrea L, O’Keeffe M, et al. The Burden of Pain: A Societal Impact of Pain (SIP) Book of Evidence. European Pain Federation; 2024.
- Rosenberger DC, Blechschmidt V, Timmerman H, Wolff A, Treede RD. Challenges of neuropathic pain: focus on diabetic neuropathy. J Neural Transm. 2020 Apr 1;127(4):589–624.
- Delcour J, Griebler R. Global Burden of Disease Study zur Einschätzung der Krankheitslast: Hintergründe und Anwendungsmöglichkeiten. Factsheet. 2022;
- Abbafati C, Abbas KM, Abbasi M, Abbasifard M, Abbasi-Kangevari M, Abbastabar H, et al. Global burden of 369 diseases and injuries in 204 countries and territories, 1990–2019: a systematic analysis for the Global Burden of Disease Study 2019. The Lancet. 2020 Oct 17;396(10258):1204–22.
- Scholz J. Finally, A Systematic Classification of Pain (the ICD-11). Pract Pain Manag. 2019;19(3).
- Huskisson EC. MEASUREMENT OF PAIN. The Lancet. 1974 Nov 9;304(7889):1127–31.
- Fernandez James C, Tripathi S, Karampatou K, Gladston D V, Pappachan JM. Pharmacotherapy of Painful Diabetic Neuropathy: A Clinical Update. Sisli Etfal Hastan Tıp Bul. 2022 Mar 28;56(1):1–20.
- Valenza M, Facchinetti R, Steardo L, Scuderi C. Palmitoylethanolamide and White Matter Lesions: Evidence for Therapeutic Implications. Vol. 12, Biomolecules. MDPI; 2022 Aug 27;12(9):1191.
- Rankin L, Fowler CJ. The Basal pharmacology of palmitoylethanolamide. Int J Mol Sci. 2020 Nov 1;21(21):1–22.
- Nobili S, Micheli L, Lucarini E, Toti A, Ghelardini C, Di Cesare Mannelli L. Ultramicronized N-palmitoylethanolamine associated with analgesics: Effects against persistent pain. Pharmacol Ther. 2024 Jun 1;258.
- Scuteri D, Guida F, Boccella S, Palazzo E, Maione S, Rodríguez-Landa JF, et al. Effects of Palmitoylethanolamide (PEA) on Nociceptive, Musculoskeletal and Neuropathic Pain: Systematic Review and Meta-Analysis of Clinical Evidence. Vol. 14, Pharmaceutics. MDPI; 2022.
- Lang-Illievich K, Klivinyi C, Lasser C, Brenna CTA, Szilagyi IS, Bornemann-Cimenti H. Palmitoylethanolamide in the Treatment of Chronic Pain: A Systematic Review and Meta-Analysis of Double-Blind Randomized Controlled Trials. Vol. 15, Nutrients. Multidisciplinary Digital Publishing Institute (MDPI); 2023 Mar 10;15(6):1350.
- Schweiger V, Schievano C, Martini A, Polati L, Del Balzo G, Simari S, et al. Extended Treatment with Micron-Size Oral Palmitoylethanolamide (PEA) in Chronic Pain: A Systematic Review and Meta-Analysis. Nutrients. 2024 May 28;16(11):1653.
- Briskey D, Skinner R, Smith C, Rao A. Effectiveness of Palmitoylethanolamide (Levagen+) Compared to a Placebo for Reducing Pain, Duration, and Medication Use during Migraines in Otherwise Healthy Participants—A Double-Blind Randomised Controlled Study. Pharmaceuticals. 2024;17(2).