Protease – Wirkung, Eiweißverdauung und Bedeutung für den menschlichen Organismus
Protease – Anwendung und Qualität eingeordnet
Proteasen werden medizinisch vor allem bei einer eingeschränkten körpereigenen Enzymproduktion eingesetzt, etwa im Rahmen einer exokrinen Pankreasinsuffizienz. In diesen Fällen ist die Substitution essenziell, um eine ausreichende Eiweißverdauung und Nährstoffaufnahme sicherzustellen.
Darüber hinaus kommen Protease-Enzyme auch als Nahrungsergänzungsmittel zum Einsatz, insbesondere bei funktionellen Verdauungsbeschwerden oder eiweißreicher Ernährung. Außerdem werden Proteasen auch zur Unterstützung von chronischen Entzündungen eingesetzt, wie etwa bei aktivierten Arthrosen, Rhinosinusitis, Sehnenscheidenentzündungen oder Muskelschmerzen.
Entscheidend ist hierbei weniger die eingesetzte Wirkstoffmenge als vielmehr die Enzymaktivität, da nur diese die tatsächliche proteolytische Leistung widerspiegelt.
Hochwertige Präparate orientieren sich am physiologischen Zusammenspiel der Verdauungsenzyme und kombinieren Proteasen sinnvoll mit weiteren Enzymen. Ebenso relevant sind eine gute Verträglichkeit, geprüfte Reinheit sowie eine geeignete Darreichungsform, um die Enzymaktivität gezielt im Verdauungstrakt zur Wirkung zu bringen.
Protease – Schlüsselenzyme für Eiweißverdauung, Stoffwechsel und Medizin
Proteasen zählen zu den zentralen Enzymen des menschlichen Organismus. Sie sind an der Eiweißverdauung, an zahlreichen Stoffwechselprozessen sowie an Immun- und Reparaturmechanismen beteiligt. Ohne diese Enzyme wäre weder die Aufnahme von Aminosäuren noch der kontinuierliche Umbau körpereigener Proteine möglich. Der folgende Beitrag beleuchtet fundiert und praxisnah, was eine Protease ist, welche Wirkung Proteasen entfalten, wie sie im Körper wirken und wann eine ergänzende Zufuhr sinnvoll sein kann.
Was ist eine Protease?
Eine Protease ist ein Enzym, das Proteine (Eiweiße) spaltet. Chemisch gesehen katalysiert sie die Hydrolyse (Spaltung) von Peptidbindungen – also jener Bindungen, die einzelne Aminosäuren zu langen Proteinketten verknüpfen. Durch diesen Prozess entstehen zunächst kleinere Peptide und schließlich freie Aminosäuren, die der Körper aufnehmen und verwerten kann.
Häufig werden die Begriffe Protease, Peptidase und Proteinase synonym verwendet. Fachlich betrachtet ist Protease der Überbegriff. Peptidasen spalten kürzere Peptide, während Proteinase historisch für Endoproteasen genutzt wurde. In der modernen Biochemie hat sich jedoch der Sammelbegriff Protease etabliert.
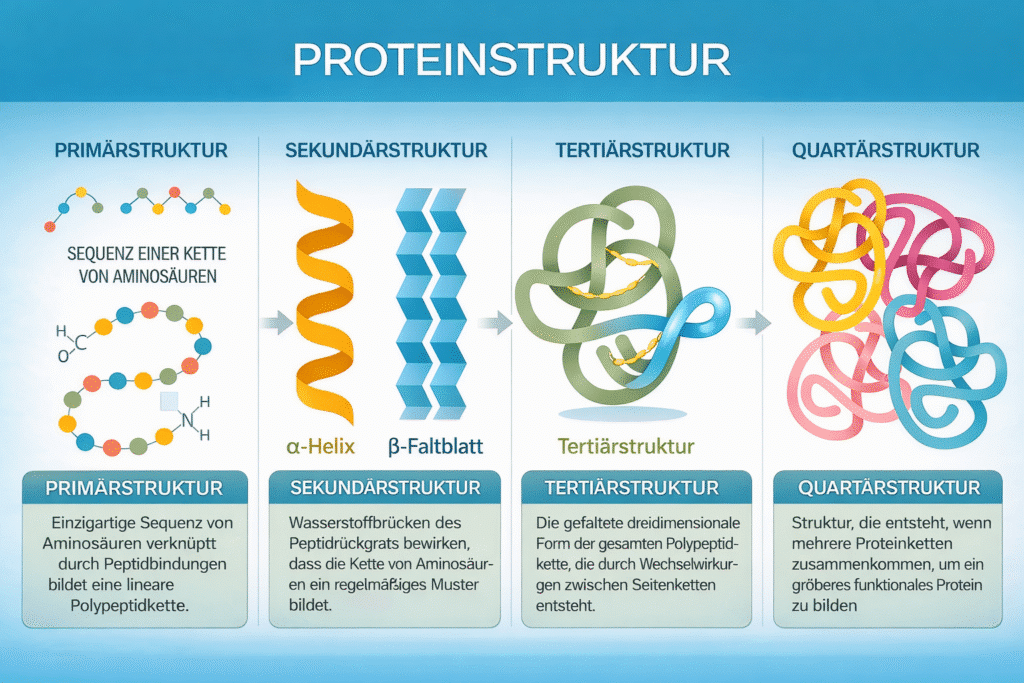
Abbildung 1. Protein Struktur: Ein Protein besteht aus einer bestimmten Anzahl an Aminosäuren, die miteinander verknüpft die Primärstruktur des Proteins ergeben. Diese Aminosäurekette dreht sich dann entweder in weiterer Folge zu einer Alpha-Helix oder Beta-Faltblatt (Sekundärstruktur). Dann faltet sich die Aminosäurekette zu einer Polypeptikette aufgrund der Wechselwirkungen zwischen den Seitenketten der Aminosäuren (Tertiärstruktur). Mehrere Polypeptidketten können sich zu einem komplexen Proteinmolekül in der Quartärstruktur verbinden.
Protease-Enzym: Warum die Proteolyse lebensnotwendig ist
Die Wirkung von Proteasen beschränkt sich nicht auf die reine Eiweißverdauung im Magen-Darm-Trakt. Vielmehr sind diese Enzyme an einer Vielzahl essenzieller biologischer Prozesse beteiligt. Durch den gezielten Abbau und Umbau von Proteinen tragen Proteasen maßgeblich dazu bei, dass der Organismus funktionsfähig und anpassungsfähig bleibt. Dazu zählen insbesondere:
- die Erneuerung von Zellen und Geweben
- die Regulation von Signalwegen
- die Anpassung des Stoffwechsels
- die Immunabwehr und Entzündungssteuerung
Diese Prozesse laufen kontinuierlich und hochreguliert ab. Proteasen sorgen dafür, dass beschädigte, fehlgefaltete oder nicht mehr benötigte Proteine abgebaut werden, während gleichzeitig neue funktionelle Proteine gebildet werden können. Auf diese Weise leisten sie einen zentralen Beitrag zur zellulären Homöostase und zur physiologischen Balance zahlreicher Organsysteme(1).
KaRazym® ist ein bewährter, natürlicher Enzymkomplex mit Bromelain, Papain, Pankreatin und Rutin – zur ernährungsphysiologischen Unterstützung bei akuten und chronischen Entzündungen und Schwellungen.
MEHR ERFAHRENFunktionen und Bedeutung von Proteasen im Körper
Proteasen und Eiweißverdauung
Die bekannteste Aufgabe von Proteasen ist die Eiweißverdauung im Magen-Darm-Trakt. Bereits im Magen beginnt Pepsin mit der Aufspaltung von Nahrungseiweißen. Im Dünndarm setzen pankreatische Proteasen wie Trypsin, Chymotrypsin und Elastase die Verdauung fort. Erst durch dieses fein abgestimmte Zusammenspiel können Aminosäuren effektiv resorbiert werden.
Proteasen im Stoffwechsel und in Zellen
Auch außerhalb des Verdauungstraktes sind Proteasen aktiv. Das Proteasom, ein komplexes Enzymsystem innerhalb der Zelle, baut fehlgefaltete oder überalterte Proteine ab. Dieser Prozess ist entscheidend für Zellgesundheit und Anpassungsfähigkeit (2).
Rolle im Immunsystem und in der Wundheilung
Proteasen regulieren Entzündungsreaktionen, aktivieren Immunbotenstoffe und sind an der Wundheilung sowie am Gewebeumbau beteiligt. Gleichzeitig wird ihre Aktivität durch körpereigene Proteaseinhibitoren streng kontrolliert, um überschießende Reaktionen zu verhindern.
Einteilung und Klassifikation von Proteasen
Einteilung nach dem Ort der Spaltung
Proteasen lassen sich unter anderem danach einteilen, an welcher Stelle der Proteinkette sie angreifen. Diese Unterscheidung ist biochemisch relevant, da sie bestimmt, wie und in welchem Schritt ein Protein abgebaut wird. Grundsätzlich unterscheidet man zwei Hauptformen:
- Endoproteasen: spalten Peptidbindungen innerhalb der Proteinkette
- Exoproteasen: spalten einzelne Aminosäuren von den Enden der Kette ab
Endoproteasen übernehmen in der Regel den ersten, groben Schritt der Eiweißspaltung, indem sie große Proteinmoleküle in kürzere Peptide zerlegen. Exoproteasen setzen anschließend an diesen Fragmenten an und bauen sie schrittweise weiter ab, bis freie Aminosäuren entstehen, die vom Körper aufgenommen und verwertet werden können. Erst durch dieses abgestufte Zusammenspiel wird eine effiziente und vollständige Eiweißverdauung ermöglicht (3).
Einteilung nach katalytischem Mechanismus
Eine weitere wichtige Klassifikation von Proteasen erfolgt nach dem katalytischen Mechanismus, also nach der Art der chemischen Gruppe im aktiven Zentrum des Enzyms, die die Spaltung der Peptidbindung ermöglicht. Diese Einteilung ist nicht nur für das biochemische Verständnis relevant, sondern auch für medizinische und pharmakologische Fragestellungen, da sich daraus unterschiedliche Wirkprofile und Regulationsmechanismen ableiten lassen. Zu den zentralen Gruppen zählen:
- Serinproteasen (z. B. Trypsin), bei denen eine Serin-Seitenkette im aktiven Zentrum die Spaltung der Peptidbindung vermittelt. Sie spielen eine zentrale Rolle in der Verdauung, der Blutgerinnung sowie in immunologischen Prozessen.
- Cysteinproteasen (z. B. Papain), deren katalytische Aktivität auf einer reaktiven Cystein-Gruppe beruht. Diese Proteasen kommen sowohl im menschlichen Organismus als auch in Pflanzen vor und sind unter anderem an Entzündungs- und Umbauprozessen beteiligt.
- Aspartatproteasen (z. B. Pepsin), die zwei Aspartat-Reste zur Aktivierung eines Wassermoleküls nutzen. Sie sind vor allem im sauren Milieu des Magens aktiv und übernehmen dort die initiale Spaltung von Nahrungseiweißen.
- Metalloproteasen (z. B. Matrix-Metalloproteasen), deren Aktivität von einem Metallion – meist Zink – abhängig ist. Sie sind maßgeblich am Gewebeumbau, an der Wundheilung und an entzündlichen Prozessen beteiligt und unterliegen einer besonders strengen Regulation.
- Threoninproteasen (z. B. das Proteasom), bei denen eine Threonin-Seitenkette die katalytische Funktion übernimmt. Sie sind essenziell für den intrazellulären Proteinabbau und damit für die Aufrechterhaltung der Zellfunktion und Proteinhomöostase.
Diese Klassifikation ist nicht nur biochemisch relevant, sondern auch für medizinische Anwendungen von Bedeutung (4).
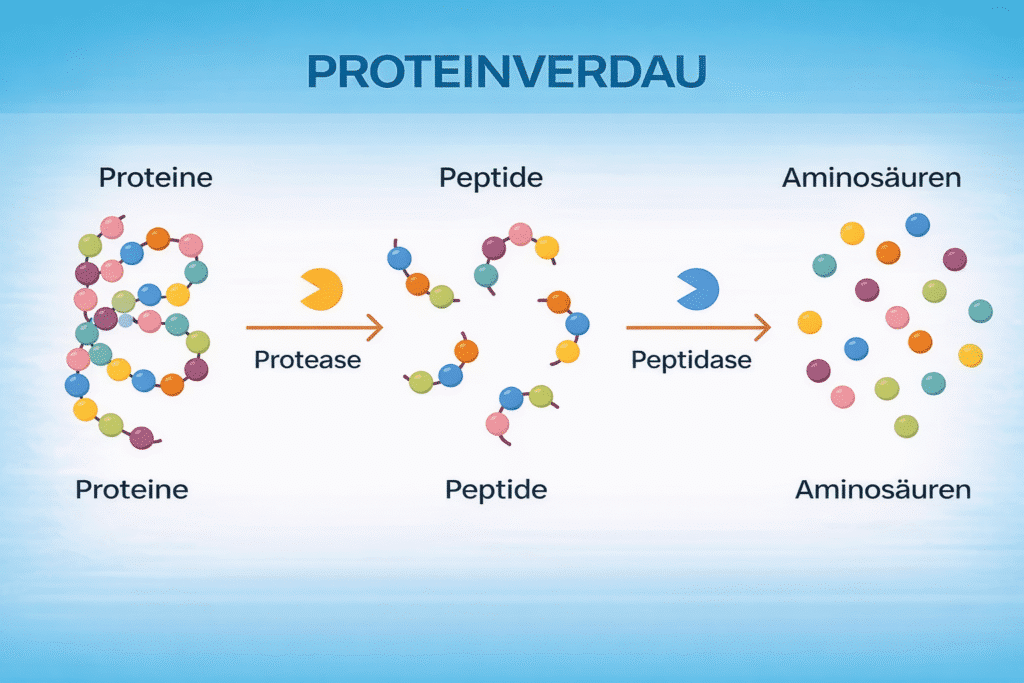
Abbildung 2. Proteinverdau: Proteine werden durch Proteasen in einzelne Peptidelemente zerschnitten. Dann zerlegen Peptidasen die Peptidketten in die einzelnen freien Aminosäuren.
Proteasen in Pflanzen, Lebensmitteln und Mikroorganismen
Neben körpereigenen Enzymen spielen auch pflanzliche Proteasen eine relevante Rolle. Sie kommen natürlicherweise in bestimmten Lebensmitteln vor und zeichnen sich durch eine ausgeprägte proteolytische Aktivität aus. Aufgrund ihrer Herkunft und ihrer vergleichsweise guten Stabilität werden sie seit Langem sowohl ernährungsphysiologisch als auch ergänzend eingesetzt. Besonders bekannt sind dabei:
- Papain aus der Papaya (5)
- Bromelain aus der Ananas (6)
Beide Enzyme gehören zur Gruppe der Cysteinproteasen und sind in der Lage, Proteine effektiv in kleinere Peptide zu spalten. In frischer, roher Form tragen papaya- und ananashaltige Lebensmittel daher zur Unterstützung der Eiweißverdauung bei.
Werden die pflanzlichen Proteasen in magensaftresistenten Formulierungen wie z.B. magensaftresistente Tabletten oder Kapseln verarbeitet, können diese Proteasen auch im Dünndarm über die Schleimhaut aufgenommen werden und eine systemische Wirkung ausüben. So wird der Einfluss dieser Proteasen auf Entzündungsreaktionen und das Immunsystem erklärt.
Darüber hinaus werden Papain und Bromelain aufgrund ihrer definierten enzymatischen Eigenschaften auch gezielt gewonnen und weiterverarbeitet, wobei Reinheit, Aktivität und Herkunft für die fachliche Bewertung entscheidend sind.
Protease und gestörte Eiweißverdauung
Diese Enzyme sind hitzeempfindlich und entfalten ihre Wirkung vor allem in roher Form. Auch Mikroorganismen produzieren Proteasen, die in der Lebensmitteltechnologie, etwa bei Fermentationsprozessen, genutzt werden.
Eine unzureichende Proteaseaktivität kann zu einer gestörten Eiweißverdauung führen. In diesem Fall werden Nahrungseiweiße nicht vollständig in resorbierbare Aminosäuren zerlegt, was sowohl lokale als auch systemische Folgen haben kann. Typische Beschwerden äußern sich zunächst im Magen-Darm-Trakt, können bei längerem Bestehen jedoch den gesamten Organismus betreffen. Häufig beobachtet werden dabei:
- Völlegefühl und Blähungen, die durch unvollständig gespaltene Proteine und nachfolgende bakterielle Fermentationsprozesse entstehen
- Durchfälle oder Fettstuhl, als Ausdruck einer gestörten Nährstoffverwertung und veränderten Darmfunktion
- Müdigkeit und Nährstoffmängel, da essenzielle Aminosäuren nicht ausreichend zur Verfügung stehen
- Muskelabbau bei chronischem Verlauf, wenn der Körper zur Deckung seines Bedarfs vermehrt körpereigene Proteinreserven mobilisiert
Diese Symptomatik verdeutlicht, dass eine gestörte Eiweißverdauung nicht nur ein lokales Verdauungsproblem darstellt, sondern langfristig auch den Protein- und Energiestoffwechsel beeinträchtigen kann. Gerade bei persistierenden Beschwerden ist daher eine gezielte Abklärung der Enzymfunktion sinnvoll (7).
Protease als Nahrungsergänzung oder Arzneimittel
Bei der Auswahl eines Protease-Präparates spielt die Qualität eine entscheidende Rolle, da Enzyme nur dann wirksam sein können, wenn ihre Aktivität im Verdauungstrakt tatsächlich erhalten bleibt. Für die fachliche Beurteilung haben sich dabei mehrere Kriterien etabliert, die eine zuverlässige Einordnung ermöglichen:
- klar definierte Enzymaktivität statt reiner Gewichtsangaben, da ausschließlich die enzymatische Leistung darüber entscheidet, in welchem Ausmaß Proteine tatsächlich gespalten werden können
- Kombination mehrerer Enzyme für eine synergistische Wirkung, weil die Eiweißverdauung physiologisch im Zusammenspiel mit weiteren Verdauungsenzymen erfolgt und erst dieses Zusammenspiel eine effiziente Nährstoffverwertung ermöglicht
- gute Verträglichkeit und geprüfte Reinheit, um auch bei sensiblen Personen eine sichere Anwendung zu gewährleisten und unnötige Belastungen durch Zusatzstoffe zu vermeiden
- geeignete Darreichungsform zum Schutz vor Magensäure, da Proteasen als Eiweiße empfindlich gegenüber saurem Milieu sind und ihre Aktivität nur dann entfalten können, wenn sie den Wirkort in funktioneller Form erreichen
Diese Qualitätsmerkmale tragen wesentlich dazu bei, ob ein Protease-Präparat in der Praxis tatsächlich einen sinnvollen Beitrag zur Unterstützung der Eiweißverdauung leisten kann (8).
Nebenwirkungen und Risiken
Proteasen gelten bei sachgerechter Anwendung grundsätzlich als gut verträglich. Dennoch gibt es bestimmte Situationen, in denen eine erhöhte Aufmerksamkeit erforderlich ist. Dies betrifft insbesondere Personengruppen, bei denen aufgrund physiologischer Besonderheiten oder möglicher Wechselwirkungen eine individuelle Nutzen-Risiko-Abwägung sinnvoll ist. Besondere Vorsicht ist daher geboten bei:
- Schwangerschaft und Stillzeit, da für diese Lebensphasen nur begrenzt belastbare Daten zur Sicherheit einer zusätzlichen Enzymeinnahme vorliegen
- bestehenden Allergien (z. B. auf Papaya oder Ananas), da pflanzliche Proteasen aus diesen Quellen stammen können und in Einzelfällen allergische Reaktionen auslösen
- gleichzeitiger Einnahme bestimmter Medikamente, da proteolytische Enzyme theoretisch die Resorption oder Wirkung anderer Wirkstoffe beeinflussen können
In diesen Fällen empfiehlt sich eine fachliche Abklärung, um mögliche Risiken zu minimieren und eine sichere Anwendung zu gewährleisten (9).
Ihre Fragen, unsere Antworten
Was macht die Protease?
Proteasen spalten Proteine in Peptide und Aminosäuren und ermöglichen so Verdauung, Zellumbau und Regulation zahlreicher Körperfunktionen.
Welche Lebensmittel enthalten Proteasen?
Rohes Obst wie Papaya (Papain) und Ananas (Bromelain) enthält natürliche Proteasen.
Ist es sinnvoll, Enzyme zu nehmen?
Bei gesicherter Enzymmangelsituation oder erhöhter Belastung kann eine ergänzende Zufuhr sinnvoll sein. Eine individuelle Abklärung ist empfehlenswert.
Wo findet man Protease im Körper?
Proteasen werden unter anderem im Magen, in der Bauchspeicheldrüse, im Darm sowie in nahezu allen Zellen gebildet.

Quellenverzeichnis
- Rawlings ND, Barrett AJ, Finn R. Twenty years of the MEROPS database of proteolytic enzymes, their substrates and inhibitors. Nucleic Acids Res [Internet]. 2016 [cited 2025 Dec 30];44(D1):D343–50. Available from: https://pubmed.ncbi.nlm.nih.gov/26527717/
- Collins GA, Goldberg AL. The Logic of the 26S Proteasome. Cell [Internet]. 2017 May 18 [cited 2025 Dec 30];169(5):792–806. Available from: https://pubmed.ncbi.nlm.nih.gov/28525752/
- Barrett AJ, Rawlings ND, Woessner JF. Handbook of Proteolytic Enzymes: Second Edition. Handbook of Proteolytic Enzymes: Second Edition. 2004 Jun 30;1:1–1140.
- Rawlings ND, Barrett AJ. Evolutionary families of metallopeptidases. Methods Enzymol [Internet]. 1995 Jan 1 [cited 2025 Dec 30];248(C):183–228. Available from: https://pubmed.ncbi.nlm.nih.gov/7674922/
- Choudhary R, Kaushik R, Chawla P, Manna S. Exploring the extraction, functional properties, and industrial applications of papain from Carica papaya. J Sci Food Agric [Internet]. 2025 Feb 1 [cited 2025 Dec 30];105(3):1533–45. Available from: https://pubmed.ncbi.nlm.nih.gov/39077990/
- Hikisz P, Bernasinska-Slomczewska J. Beneficial properties of bromelain. Nutrients. 2021;13(12). Available from: https://pubmed.ncbi.nlm.nih.gov/34959865/
- López-Otín C, Bond JS. Proteases: Multifunctional Enzymes in Life and Disease. J Biol Chem [Internet]. 2008 Nov 7 [cited 2025 Dec 30];283(45):30433. Available from: https://pmc.ncbi.nlm.nih.gov/articles/PMC2576539/
- Domínguez-Muñoz JE. Pancreatic enzyme replacement therapy: exocrine pancreatic insufficiency after gastrointestinal surgery. HPB [Internet]. 2009 Dec [cited 2025 Dec 30];11(Suppl 3):3–6. Available from: https://pubmed.ncbi.nlm.nih.gov/20495625/
- Pereira IC, Sátiro Vieira EE, de Oliveira Torres LR, Carneiro da Silva FC, de Castro e Sousa JM, Torres–Leal FL. Bromelain supplementation and inflammatory markers: A systematic review of clinical trials. Clin Nutr ESPEN [Internet]. 2023 Jun 1 [cited 2025 Dec 30];55:116–27. Available from: https://pubmed.ncbi.nlm.nih.gov/37202035/









